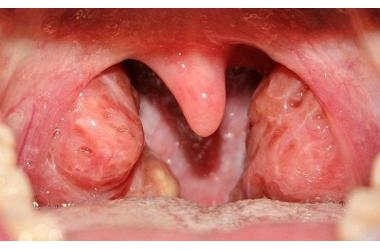
Hạ lipid máu
Giá bán: Liên hệ
- Xuất xứ: Pháp
- Tình trạng: Còn hàng
Qui cách đóng gói: 2 vỉ, mỗi vỉ 15 viên.
Thành phần: Fenofibrate 200mg
Nhóm: Thuốc hạ mỡ máu (Hạ cholesterol)
Nhà sản xuất: Abbott (Mỹ)
Sản xuất tại Pháp
Thành phần
Hoạt chất chính: Fenofibrate (INN) 200mg
Tá dược: lactose monohydrate; magnesium stearate; tinh bột đã gelatin hóa; Natrilauril sulfate; crospovidone.
Tá dược có hoạt tính: mỗi viên chứa: 101mg Lactose monohydrate
Công dụng (Chỉ định)
Thuốc được chỉ định điều trị các trường hợp tăng cholesterol và tăng triglyceride máu đơn thuần hoặc phối hợp (rối loạn lipid máu bao gồm cả rối loạn lipoprotein huyết các dạng IIa, IIb, III, IV và V) ở bệnh nhân không đáp ứng với chế độ ăn kiêng và các biện pháp điều trị không dùng thuốc khác (ví dụ: biện pháp làm giảm thể trọng hoặc tăng cường hoạt động thể lực), đặc biệt khi có những bằng chứng có nguy cơ khác kèm theo như là cao huyết áp và hút thuốc lá.
Điều trị tăng lipoprotein máu thứ phát cũng là một chỉ định nếu sự bất thường lipoprotein máu dai dẳng cho dù đã điều trị căn nguyên (ví dụ: rối loạn lipid máu trong đái tháo đường). Chế độ ăn kiêng trước khi dùng thuốc vẫn phải tiếp tục.
Liều dùng
Nên theo dõi đáp ứng của điều trị bằng cách xác định các chỉ số huyết thanh. Nếu không đạt được đáp ứng thỏa đáng sau vài tháng điều trị (ví dụ: 3 tháng), nên cân nhắc bổ sung thêm hoặc dùng biện pháp điều trị khác.
Liều dùng:
Người lớn:
Liều khuyến cáo là 200mg mỗi ngày dưới dạng một viên nang Lipanthyl 200M.
Nhóm đối tượng đặc biệt
Người cao tuổi:
Với bệnh nhân cao tuổi, không suy thận, khuyến cáo dùng liều thông thường cho người lớn.
Suy thận:
Cần giảm liều với các bệnh nhân suy thận. Khuyến cáo không dùng Fenofibrate với các bệnh nhân bị bệnh thận mãn tính nặng.
Suy gan:
Không khuyến cáo sử dụng Lipanthyl 200M với bệnh nhân suy gan do còn thiếu dữ liệu.
Trẻ em:
Chưa xác định được an toàn và hiệu quả của Fenofibrate với trẻ em và thanh thiếu niên dưới 18 tuổi. Không có dữ liệu hiện hành. Vì thế không khuyên cáo dùng fenofibrate với trẻ em dưới 18 tuổi.
Cách dùng:
Viên nang nên được uống trong bữa ăn.
Không sử dụng trong trường hợp sau (Chống chỉ định)
Không dùng thuốc trong những trường hợp sau đây:
- Suy gan (bao gồm xơ gan ứ mật và bất thường về chức năng gan dai dẳng không rõ nguyên nhân),
- Bệnh túi mật,
- Bệnh thận mãn tính nghiêm trọng,
- Trẻ em
- Thời kỳ cho con bú
- Viêm tụy cấp tính hoặc mạn tính ngoại trừ trường hợp viêm tụy cấp do tăng triglycerid máu nặng,
- Tiền sử dị ứng với ánh sáng hoặc nhiễm độc với ánh sáng khi điều trị với các fibrate hoặc ketoprofen
- Mẫn cảm với dược chất hoặc bất cứ thành phần tá dược nào được liệt kê trong mục “THÀNH PHẦN CHO MỖI VIÊN”.
Lưu ý khi sử dụng (Cảnh báo và thận trọng)
Thuốc không thay thế được chế độ ăn kiêng, cần dùng thuốc đều đặn. phải thường xuyên kiểm tra công thức máu.
Tăng lipid máu thứ phát:
Nguyên nhân của tăng lipid máu thứ phát như là bị bệnh tiểu đường type 2 không kiểm soát được, suy giáp, hội chứng thận hư, rối loạn protein máu, bệnh lý gan tắc nghẽn, đang dùng dược lý trị liệu, nghiện rượu, các tình trạng này nên cân nhắc điều trị triệt để trước khi điều trị với fenofibrate. Với các bệnh nhân tăng lipid máu đang sử đụng các oestrogen hoặc các liệu pháp tránh thai có chứa oestrogen thì nên được xác định rõ ràng rằng liệu tăng lipid máu là nguyên phát hay thứ phát (có thể chỉ số lipid tăng là do uống oestrogen).
Chức năng gan:
Cũng như các thuốc giảm lipid khác, nồng độ transaminase tăng đã ghi nhận được trên một số bệnh nhân. Trong đa số trường hợp, sự tăng này là thoáng qua, nhỏ và không có triệu chứng. Khuyến cáo theo dõi nồng độ transaminase định kỳ mỗi 3 tháng trong 12 tháng điều trị đầu tiên và định kỳ sau đó. Cần thận trọng với các bệnh nhân có tăng nồng độ transaminase tiến triển và nên ngừng điều trị nếu nồng độ AST (SGOT) và ALT (SGPT) tăng lên hơn 3 lần giới hạn trên của mức bình thường. Khi các triệu chứng cho thấy có xảy ra viêm gan (ví dụ như vàng da, ngứa), và chẩn đoán này được xác nhận bởi xét nghiệm, thì nên ngừng dùng fenofibrate.
Tụy:
Viêm tụy đã được ghi nhận ở các bệnh nhân dùng fenofibrate (xem mục Chống chỉ định và Tác dụng không mong muốn). Điều này cho thấy thất bại trong điều trị ở những bệnh nhân tăng triglyceride máu nghiêm trọng, đây là ảnh hưởng trực tiếp của thuốc hoặc là hiện tượng thứ cấp do sỏi đường mật hoặc bùn gây tắc nghẽn ống mật chủ gây ra.
Cơ:
Độc tính cơ, bao gồm các trường hợp tiêu cơ vân hiếm gặp, cố hoặc không kèm với suy thận, đã được báo cáo khi dùng các fenofibrate và các thuốc làm giảm lipid khác. Tỷ lệ mắc các rối loạn này tăng lên với các trường hợp albumin máu thấp và đã có tiền sử suy thận.
Bệnh nhân có các yếu tố tiềm ẩn của bệnh cơ và/hoặc tiêu cơvân bao gồm: trên 70 tuổi, tiền sử cá nhân hoặc gia đình có rối loạn di truyền về cơ, suy thận, suy giáp và nghiện rượu, những điều này có thể tăng nguy cơ tiến triển tiêu cơ vân. Đối với những bệnh nhân này, nên cân nhắc cẩn trọng giữa lợi ích và nguy cơ khi dùng fenofibrate.
Nên nghi ngờ có độc tính cơ ở các bệnh nhân có đau cơ lan tỏa, viêm cơ, co cứng cơ và yếu cơ và/hoặc tăng CPK đáng kể (nồng độ vượt quá 5 lần mức bình thường). Trong trường hợp này nên ngưng điều trị với fenofibrate.
Nguy cơ độc tính cơ có thể tăng lên nếu phối hợp với fibrate khác hoặc một thuốc ức chế HMG-CoA reductase, đặc biệt là các trường hợp đã từng bị bệnh về cơ. Do đó, kê đơn phối hợp fenofibrate với thuốc ức chế HMG-CoA reductase hoặc một fibrate khác chỉ nên được áp dụng với các bệnh nhân bị rối loạn lipid máu hỗn họp nặng và có nguy cơ tim mạch cao mà chưa có tiền sử bệnh về cơ và cần theo dõi chặt chẽ tiềm năng độc tính cơ.
Chức năng thận:
Nên ngưng điều trị với các trường hợp có chỉ số creatinine tăng > 50% ULN (giới hạn trên của mức bình thường). Khuyến cáo đo nồng độ creatinine trong 3 tháng đầu kể từ khi bắt đầu điều trị và định kỳ sau đó (các liều khuyến cáo, xem mục 4.2 Liều lượng và cách dùng).
Tá dược:
Do thuốc có chứa lactose, các bệnh nhân có vấn đề về di truyền hiếm gặp không dung nạp galactose, thiếu hụt Lapp lactase hoặc kém hấp thu glucose-galactose không nên dùng thuốc này.
Tác dụng không mong muốn (Tác dụng phụ)
Các báo cáo ADR thường gặp nhất trong quá trình điều trị vói fenofibrate là rối loạn tiêu hóa, dạ dày hoặc ruột.
Các tác dụng không mong muốn sau đây đã quan sát được trong các thử nghiệm lâm sàng có đối chứng placebo (giả dược) (n=2344) có tần số được chỉ ra dưới đây:
|
DRA trên các nhóm hệ thống cơ thể |
Phổ biến ≥ 1/100, < 1/10 |
Không phổ biến ≥ 1/1,000, < 1/100 |
Hiếm ≥ 1/10,000, < 1/1,000 |
Rất hiếm < 1/10,000 bao gồm cả các báo cáo riêng biệt |
|
Rối loạn hệ máu và bạch huyết |
- |
- |
Giảm Haemoglobin Giảm số lượng bạch cầu |
- |
|
Rối loạn hệ miễn dịch |
- |
- |
Dị ứng |
- |
|
Rối loạn hệ thần kinh |
- |
Đau đầu |
Mệt mỏi, chóng mặt |
- |
|
Rối loạn mạch |
- |
Nghẽn mạch (tắc mạch phổi, huyết khối tĩnh mạch sâu)* |
- |
- |
|
Rối loạn dạ dày-ruột |
Các triệu chứng cơ năng và thực thể dạ dày-ruột (đau bụng, nôn, buồn nôn, tiêu chảy, đầy hơi) |
Viêm tụy* |
- |
- |
|
Các rối loạn gan mật |
Tăng transaminase (xem mục 4.4) |
Bệnh sỏi mật (xem mục 4.4) |
Viêm gan |
- |
|
Rối loạn da và mô dưới da |
- |
Tăng nhạy cảm trên da (ví dụ: phát ban, ngứa, mày đay) |
Rụng tóc Phản ứng nhạy cảm ánh sáng |
- |
|
Các rối loạn về cơ, mô liên kết và xương |
- |
Rối loạn cơ (ví dụ: đau cơ, viêm cơ, các incơn đau cơ và yếu cơ) |
- |
- |
|
Các rối loạn về ngực và hệ thống sinh sản |
- |
Rối loạn chức năng tình dục |
- |
- |
|
Xét nghiệm |
- |
Tăng Creatinin máu |
Tăng ure máu |
- |
* Trong nghiên cứu FIELD, thử nghiệm ngẫu nhiên có đối chứng giả dược trên 9.795 bệnh nhân bị đái tháođường type 2,thấy tăng có ýnghĩa thống kê cáctrường hợp viêm tụy với các bệnh nhân dùng fenofibrate so với các bệnh nhân dùng giả dược (0.8% so với 0.5%, p= 0.0031). Cũng trong nghiên cứu này, đã ghi nhận được sự gia tăng có ý nghĩa thống kê về tỷ lệ mắc bệnh nghẽn mạch phổi (0,7% ở nhóm giả dược so với 1.1% ở nhóm dùng fenofibrate; p= 0.022) và tăng không đáng kể huyết khối tĩnh mạch sâu (giả dược: 1.0% [48/4.900 bệnh nhân] so với fenofibrate 1.4% [67/4.895 bệnh nhân];p= 0.074).
a Ngoài các sự kiện đã được báo cáo trong các thử nghiệm lâm sàng, các tác dụng không mong muốn sau đây đã được báo cáo tự phát khi sử dụng Lipanthyl 200M trong quá trình hậu mãi. Chưa ước tính được tần số chính xác dựa trên các dữ liệu hiện có và do đó được xếp là “Không rõ”.
- Các rối loạn hô hấp, ngực và trung thất: Bệnh phổi kẽ.
- Các rối loạn cơ, mô liên kết và các rối loạn xương: Tiêu cơ vân.
- Các rối loạn gan mật: vàng da, biến chứng của sỏi mật (ví dụ: viêm túi mật, viêm đường mật, cơn đau ống mật).
- Rối loạn da và mô dưới da: phản ứng nghiêm trọng ở da (vd: hồng ban đa dạng, hội chứng Stevens Johnson, hoại tử thượng bì nhiễm độc)
Tương tác với các thuốc khác
Thuốc uống chống đông:
Fenofibrate làm tăng tác dụng của thuốc uống chống đông và có thể làm tăng nguy cơ chảy máu. Khuyến cáo giảm liều của thuốc uống chống đông khoảng một phần ba khi bắt đầu điều trị và sau đó nếu cần thì điều chỉnh liều theo INR (tỉ lệ chuẩn quốc tế).
Cyclosporin:
Đã ghi nhận được một vài trường hợp suy giảm chức nặng thận thuận nghịch nghiêm trọng khi dùng đồng thời fenofibrate và cyclosporine. Chức năng thận ở những bệnh nhân này cần được giám sát chặt chẽ và ngừng điều trị với fenofibrate trong các trường hợp có thay đổi nghiêm trọng chỉ số xét nghiệm.
Các thuốc ức chế HMG-CoA reductase và các fenofibrate khác:
Nguy cơ độc tính cơ tăng lên nếu phối hợp fibrate với các thuốc ức chế HMG-CoA reductase hoặc với các fibrate khác. Khi sử dụng sự phối hợp này nên thận trọng và theo dõi chặt chẽ các dấu hiệu về độc tính với cơ trên bệnh nhân (xem mục Cảnh báo và thận trọng đặc biệt khi sử dụng).
Các Glitazone:
Đã ghi nhận được một số trường HDL-cholesterol thuận nghịch khi dùng đồng thời fenofibratte và các glitazone. Vì vậy khuyến cáo theo dõi HDL-cholesterol nếu dùng sự kết hợp trên và ngừng dùng nếu HDL-cholesterol quá thấp.
Các enzyme Cytochrome P450:
Các nghiên cứu in vitro sử dụng các tiểu thể gan người cho thấy rằng fenofibrate và acid fenofibric không ức chế các đồng phân cytochrome (CYP) P450 như CYP3A4, CYP2D6, CYP2E1, hoặc CYP1A2. Ở nồng độ điều trị thuốc ức chế yếu CYP2C19 và CYP2A6, và ức chế mức độ nhẹ đến trung bình lên CYP2C9.
Bệnh nhân dùng phối hợp fenofibrate và các thuốc chuyến hóa qua CYP2C19, CYP2A6 và đặc biệt là CYP2C9 có chỉ số điều trị hẹp nên được theo dõi cẩn trọng và nếu cần thiết thì khuyến cáo giảm liều các thuốc này.
Bảo quản
Bảo quản thuốc trong bao bì gốc, để tránh ẩm. Bảo quản dưới 30°C
Lái xe
Lipanthyl 200M không ảnh hưởng hoặc có ảnh hưởng không đáng kể lên khả năng lái xe và điều khiển máy móc.
Thai kỳ
Mang thai:
Chưa có dữ liệu đầy đủ về việc sử dụng fenofibrate ở phụ nữ mang thai. Các nghiên cứu trên động vật đã không cho thấy bất kỳ tác dụng gây quái thai nào. Với liều độc cho bà mẹ thì cho thấy ảnh hưởng lên phôi thai. Chưa biết đến nguy cơ tiềm ẩn đối với con người. Vì vậy, chỉ dùng Lipanthyl 200M trong thời kỳ mang thai sâu khi đánh giá cẩn trọng giữa lợi ích và nguy cơ.
Cho con bú: chưa có dữ liệu cho thấy liệu fenofibrate và/hoặc các chất chuyển hóa của nó có bài tiết qua sữa mẹ hay không. Rủi ro đối với trẻ bú mẹ chưa được loại trừ.
Vì vậy, không nên dùng fenofibrate khi đang cho con bú
Đóng gói
Viên nang cứng
Hộp 2 vỉ x 15 viên nang hoặc hộp 3 vỉ x 10 viên nang.
Hạn dùng
36 tháng kể từ ngày sản xuất
Quá liều
Chỉ ghi nhận được rất ít các trường hợp quá liều. Trong đa số trường hợp không ghi nhận được các triệu chứng quá liều
Không có thuốc giải độc đặc hiệu. Nếu nghi ngờ quá liều thì nên điều trị triệu chứng và tiến hành các biện pháp hỗ trợ khi cần. Fenofibrate không bị loại trừ khi thẩm tích máu.
Dược lực học
Nhóm dược lý: Các chất làm giảm lipid huyết thanh/Cholesterol và điều chỉnh Triglyceride/các Fibrate ATC Code: C10 AB 05
Fenofibrate là dẫn chất của acid fibric, chất được báo cáo là có tác dụng làm thay đổi mức lipid ở người thông qua việc hoạt hóa peroxisome Proliferator Activated Receptor type α (PPARα).
Thông qua việc hoạt hóa PPARα, fenofibrate làm tăng thủy phân lipid và đào thải các tiểu phân giàu triglyceride khỏi huyết tương nhờ hoạt hóa lipoprotein lipase và giảm sản xuất apoprotein C-III. Việc hoạt hóa PPARα cũng làm tăng tổng hợp apoprotein AI và AII.
Hiệu quả khởi đầu nêu trên đối với lipoprotein dẫn đến làm giảm LDL và VLDL có chứa apoprotein B và làm tăng HDL có chứa apoprotein AI và AII.
Thêm vào đó, thông qua việc làm thay đổi tổng họp và dị hóa các hợp phần của VLDL, fenofibrate, làm tăng độ thanh thải LDL và giảm LDL tỷ trọng thấp, các chất này thường có hàm lượng cao trong các dạng tăng sinh lipoprotein vữa xơ tại mạch, một dạng rối loạn thường gặp ở các bệnh nhân có nguy cơ về bệnh mạch vành tim.
Trong các thử nghiệm lâm sàng với fenofibrate, cholesterol toàn phần giảm từ 20 đến 25%, các triglyceride từ 40 đến 55% vả HDL cholesterol tăng từ lo đến 30%.
Với các bệnh nhân tăng cholesterol máu, khi mức cholesterol giảm từ 20 đến 35%, hiệu quả tổng thể về các giá trị cholesterol tạo nên một sự giảm tỷ lệ cholesterol toàn phần so với HDL cholesterol, LDL cholesterol so với HDL cholesterol, hoặc Apo B so với Apo AI, tất cả những điều này là dấu hiệu của nguy cơ xơ cứng động mạch.
Có bằng chứng cho rằng điều trị với fenofibrate có thể làm giảm nguy cơ tim mạch nhưng chưa cho thấy rằng giảm được mọi nguyên nhân tử vong nguyên phát hoặc thứ phát của bệnh tim mạch.
Nghiên cứu Hành động Kiểm soát Nguy cơ Tim mạch trong Bệnh tiểu đường (ACCORD) là một nghiên cứu ngẫu nhiên có đối chứng giả dược trên 5518 bệnh nhân đái tháo đường type 2 điều trị với fenofibrate có bổ sung thêm simvastatin. Điều trị với fenofibrate có thêm simvastatin đã không cho thấy bất kỳ dấu hiệu khác biệt nào đáng kể so với simvastatin đơn trị liệu trong kết quả tổng hợp về nhồi máu cơ tim không gây tử vong, đột quỵ không gây tử vong, và tử vong do tim mạch (tỷ số nguy cơ [HR] 0.92, 95% CI 0.79 - 1.08, p= 0.32; giảm nguy cơ tuyệt đối: 0.74%). Trong phân nhóm đã xác định trước của các bệnh nhân bị rối loạn lipid máu, được định nghĩa là đối tượng có phần thấp nhất là HDL-C (≤ 34mg/dl hoặc 0.88 mmol/L) và phần cao nhất là TG ( >= 204mg/ dl hoặc 2.3 mmol/L) ở ngưỡng cơ bản, điều trị với fenofibrate có kèm simvastatin cho thấy giảm tương đối là 31% so với simvastatin đơn trị liệu cho kết quả tổng hợp ban đầu là (tỷ số nguy cơ [HR] 0.69, 95% CI 0.49 - 0.97, p=0.03; giảm nguy cơ tuyệt đối: 4.95%). Số liệu phân tích của phân nhóm được xác định trước đã chỉ ra sự tác động điều trị theo giới (p=0.01) chỉ ra rằng sự kết hợp điều trị này đem lại lợi ích trên nam giới (p=0.037) nhưng trong kết luận ban đầu nguy cơ tiềm ẩn cao hơn ở nữ giới khi được điều trị phối hợp so với simvastatin đơn trị liệu (p=0.069). Điều này đã không quan sát được với các bệnh nhân rối loạn lipid máu ở các phân nhóm nói trên của nhưng cũng không có bằng chứng rõ ràng về lợi ích với những phụ nữ bị rối loạn lipid máu được điều trị phối hợp giữa fenofibrate và simvastatin, và không thể loại bỏ tác hại có thể có với phân nhóm này. Các kết quả của nghiên cứu can thiệp chứng vữa xơ do tiểu đường (DAIS) cho thấy rằng fenofibrate làm giảm đáng kể sự tiến triển của xơ vữa động mạch chính ở những bệnh nhân mắc bệnh tiểu đường type 2 và tăng lipoprotein máu. DAIS là nghiên cứu mù đôi, ngẫu nhiên, có đối chiếu giả dược trên 418 bệnh nhân đái tháo đường type 2 và tăng lipoprotein máu (total cholesterol trung bình là 5.57 mmol/L, các triglyceride 2.54 mmol/L, LDL cholesterol 3.37 mmol/L, HDL cholesterol 1.03 mmol/L). Điều trị với fenofibrate trung bình 38 tháng cho thấy giảm đáng kể sự tiến triển của tổn thương động mạch vành với tiêu chí đánh giá chụp định lượng động mạch vành là 40%.
Sự lắng cặn cholesterol ngoài thành mạch (gân và sinh u vàng) có thể được giảm đáng kể hoặc thậm trí loại bỏ hoàn toàn trong quá trình điều trị với fenofibrate.
Các bệnh nhân bị tăng fibrinogen được điều trị với fenofibrate cho thấy giảm đáng kể chỉ số này, và tăng chỉ số Lp(a). Các chất thể hiện cho quá tình viêm như C Reactive Protein cũng giảm khi điều trị với fenofibrate.
Ảnh hưởng của uricosuric lên fenofibrate dẫn đến giảm nồng độ acid uric khoảng 25% đây là lợi ích thêm vào cho các bệnh nhân bị rối loạn lipid máu có tăng uric máu. Fenofibrate đã được chứng minh là có tác dụng chống kết tập tiểu cầu ở động vật và trong một nghiên cứu lâm sàng đã cho thấy việc giảm kết tập tiểu cẩu gây ra bởi ADP, acid arachidonic và epinephrine.
Dược động học
Hấp thu:
Nồng độ tối đa trong huyết tương (Cmax) đạt được trong vòng 4 đến 5 giờ sau khi uống. Nồng độ trong huyết tương ổn định trong suốt quá trình điều trị liên tục ở mọi cá thể. Fenofibrate tăng hấp thu khi uống trong bữa ăn.
Phân bố:
Acid Fenofibric gắn mạnh với albumin huyết tương (trên 99%).
Chuyển hóa và thải trừ:
Sau khi uống, fenofibrate nhanh chóng bị thủy phân bởi các esterase thành chất chuyển hóa hoạt động là acid fenofibric.
Không phát hiện được fenofibrate nguyên dạng trong huyết tương. Fenofibrate không phải là chất nền của CYP3A4. Không bị chuyển hóa ở microsome gan.
Thuốc được thải trừ chủ yếu qua nước tiểu. Thuốc được thải trừ hoàn toàn trong vòng 6 ngày. Fenofibrate được thải trừ chủ yếu ở dạng acid fenofibric và glucurono-conjugate. Với các bệnh nhân cao tuổi, độ thanh thải huyết tương với acid fenofibric không đổi. Các nghiên cứu dược động học sau khi uống liều đơn hoặc điều trị dài ngày đã cho thấy thuốc không tích lũy.
Acid fenofibric không bị loại trừ khi thẩm tích máu.
Thời gian bán thải trong huyết tương của acid fenofibric là khoảng 20 giờ.